Авторы: О.Д. Захаров, Е.Ю. Рыбалкина, М.А. Волкова, А.А. Ставровская
ГУ РОНЦ им. Н.Н. Блохина РАМН, Москва
Резюме
Множественной лекарственной устойчивостью (МЛУ) называют резистентность клеток к ряду лекарственных препаратов, различающихся по химической структуре и механизму действия. Наиболее изученным фактором, определяющим наличие у клетки феномена МЛУ, являются белки из семейства АВС-транспортеров. По данным литературы, признана роль в развитии феномена МЛУ Pgp, MRP1, BCRP, а также LRP. Мы определяли экспрессию данных белков у первичных больных ОМЛ (кроме М3). Экспрессия данных белков наблюдалась у 64,3, 46,4, 64,3 и 42,9% больных соответственно. Бластные клетки всех больных, не ответивших на терапию, экспрессировали более одного маркера МЛУ, у 80% резистентных больных отмечена экспрессия трех и четырех маркеров, в то время как в группе чувствительных больных 1–2 маркера экспрессировались у 83% пациентов.
Ключевые слова: ОМЛ, Pgp, MRP1, BCRP, LRP
За последние годы достигнут несомненный прогресс в изучении острых миелоидных лейкозов (ОМЛ). Благодаря исследованиям патологов, клиницистов, генетиков раскрыты некоторые механизмы патогенеза, определены факторы прогноза. Все это привело к тому, что заболевание, бывшее фатальным для 100% больных, в настоящее время расценивается как потенциально излечиваемое. При использовании современных схем ПХТ 5-летняя безрецидивная выживаемость составляет 45–50%, проведение аллогенной трансплантации гемопоэтических стволовых клеток увеличивает этот показатель до 55–60%.Основной задачей, стоящей перед клиницистом при лечении первичного больного с ОМЛ, является достижение полной клинико-гематологической ремиссии. Современная терапия ОМЛ позволяет получить полные ремиссии у 65–80% первичных больных. По данным отечественных исследователей (Российская группа по изучению острых лейкозов), этот показатель составляет 64% [1]. Несмотря на очевидные успехи в лечении острых нелимфобластных лейкозов (ОНЛЛ), приблизительно у 10–20% пациентов при применении стандартной химиотерапии не удается получить полной ремиссии. Данная группа больных представляет большую клиническую проблему, так как эффективность схем второй линии химиотерапии, основанных, главным образом , на высоких дозах цитарабина, не превышает 20%. Использование новых препаратов, таких как ингибиторы топоизомеразы II (топотекан), производные платины (карбоплатин), флударабин, не улучшило ситуацию. Применение столь агрессивного метода лечения, как аллогенная трансплантация костного мозга, позволяет надеяться на долговременную выживаемость у 10% первично-резистентных больных. Таким образом, первичная резистентность, т.е. отсутствие полной ремиссии после проведения 1–2 курсов современной индукционной химиотерапии в адекватных дозах, является крайне неблагоприятным фактором прогноза и представляет собой одну из основных проблем современной онкогематологии, для решения которой проводятся многочисленные исследования.
В последние годы все больший интерес исследователей привлекает феномен множественной лекарственной устойчивости (МЛУ). МЛУ называют резистентность клеток к ряду лекарственных препаратов, различающихся по химической структуре и механизму действия [2]. От момента открытия данного феномена и до наших дней ОМЛ является наилучшей экспериментальной моделью для изучения механизмов устойчивости злокачественных клеток к действию цитостатиков. Это обусловлено высокой чувствительностью клеток к химиотерапии, относительной простотой их получения и культивирования.
Наиболее изученным фактором, определяющим наличие у клетки феномена МЛУ, являются белки из семейства АВС-транспортеров (ATP Binding Cassette transporters, АТФ-зависимые транспортеры; рис. 1). Данная группа объединяет трансмембранные протеины, связывающие АТФ и использующие энергию для транспортировки некоторых молекул через все виды клеточных мембран. Семейство подразделяется на подсемейства A, B, C, D, E, F, и G в зависимости от структуры АТФ-связывающих доменов и в настоящее время насчитывает около 50 белков, 3 из которых имеют значение в развитии феномена МЛУ при ОМЛ [3, 4].
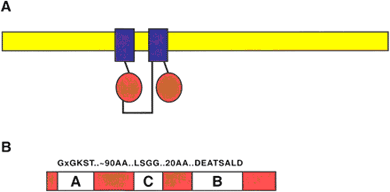
Рис. 1. Структура типичного ABC-транспортера. Желтым показана билипидная мембрана, синим – трансмембранный домен, красным – связывающая последовательность нуклеотидов
Впервые связь мембранных белков-транспортеров с феноменом МЛУ была показана в исследованиях лаборатории Victor Ling при изучении белка с молекулярной массой 170 кД, названного Р-гликопротеином (Pgp), обладавшим способностью уменьшать внутриклеточное накопление и цитотоксичность структурно и функционально различных цитостатиков [5]. Pgp кодируется геном MDR1 (относится к семейству В, международное название АВСВ1), расположенным на длинном плече хромосомы 7 (7q21). Молекула белка имеет внутри- и внеклеточный компонент и 12 раз пересекает цитоплазматическую мембрану. Его функцией являются энергозависимый транспорт (эффлюкс) за пределы клетки и уменьшение внутриклеточной концентрации большого числа ксенобиотиков, в том числе лекарственных препаратов. Кроме того, последние исследования показывают, что Pgp играет роль в увеличении апоптотического порога клетки. Pgp демонстрирует широкую специфичность к веществам с различной структурой и соответственно определяет устойчивость клеток к большому числу препаратов, таких как алкалоиды барвинка, антрациклины, эпиподофиллотоксины, таксаны, актиномицин D [6, 7]. При ОМЛ гиперэкспрессия MDR1 наблюдается, по данным разных исследователей, у 20–50% первичных больных.
Таблица 1. Экспрессия Pgp и ее влияние на частоту достижения полной ремиссии (%)
| Исследование | Экспрессия Pgp у всех больных, % | Полные ремиссии | |
| в группе Pgp+ | в группе Pgp- | ||
| J.-P. Marie и соавт. [8] (n=82) | 51 | 51 | 79 |
| P. Wood и соавт., 1996 (n=80) | 55 | 60 | 92 |
| SWOG, 1999 (n=352) | 28 | 47 | 55 |
Несмотря на предпринятые многочисленные многоцентровые исследования, роль Р-гликопротеина в развитии первичной резистентности у больных ОМЛ до сих пор остается спорной. Как видно из данных, приведенных в табл. 1, составленной по результатам многоцентровых исследований, в мировой литературе имеются противоречивые результаты: в ряде исследований отмечается достоверно больший процент достижения полных ремиссий в группе пациентов, бластные клетки которых не экспрессируют Pgp, в других работах подобного различия не отмечено [8, 9]. Были предприняты попытки связать гиперэкспрессию белка Pgp с известными прогностически неблагоприятными факторами, включая возраст, цитогенетические аберрации, гиперлейкоцитоз, уровень гемоглобина, экспрессию CD34, вторичный характер ОМЛ. Показана корреляция экспрессии Pgp с наличием маркера CD34 (по данным разных авторов, 50–70% CD34+СD38- клеток имеют Р-гликопротеин) [10, 11]. Неизвестно, оказывает ли молекула CD34 непосредственное влияние на активность Pgp. Встречаются отдельные сообщения о взаимосвязи экспрессии и функциональной активности Pgp с различными ФАБ-вариантами ОМЛ, однако на настоящий момент можно сказать, что экспрессия данного белка практически отсутствует только при остром промиелоцитарном лейкозе, отличающемся высочайшей чувствительностью к антрациклинам и служащем экспериментальной моделью для поиска путей преодоления МЛУ при других ФАБ-вариантах ОМЛ. Несомненной является связь возраста с экспрессией Pgp. В исследовании O. Legrand и соавт. [12], включившем в себя 132 пациента, Pgp определялся лишь у 17% больных моложе 35 лет, в то время как в возрастных группах 35–50 лет и старше 65 лет экспрессия составила 39 и 71% соответственно.
D. Damiani и соавт. [13] считают Pgp независимым фактором прогноза у больных с нормальным кариотипом, поскольку имеющиеся данные убедительно показывают необходимость отнесения больных с гиперэкспрессиией Pgp и нормальным кариотипом в группу неблагоприятного прогноза.
В последние годы проводятся исследования по выявлению взаимосвязи Pgp с новыми факторами прогноза, одним из которых является мутация FLT3. Показано, что бластные клетки, одновременно экспрессирующие Pgp и имеющие мутацию FLT3, отличаются сниженной апоптотической способностью в сравнении с клетками, не имеющими данной ассоциации [14]. Вслед за открытием Pgp исследование злокачественных клеток с фенотипом МЛУ, не связанным с геном MDR1, привело к открытию S.P. Cole и соавт. [15] в 1992 г. в клеточной линии мелкоклеточного рака легкого белка MRP1 (multidrug resistance-associated protein; белок, ассоциированный с множественной лекарственной устойчивостью; класс С, ген АВСС1). Этот белок с молекулярной массой 190 кДа, кодируемый геном, расположенным на хромосоме 16 (регион 16р13.1), обеспечивает резистентность примерно к тому же кругу химиопрепаратов, что и Pgp. Он транспортирует отрицательно заряженные ионы, конъюгированные с молекулой глутатиона. В норме белок MRP1 широко распространен в органах и тканях организма, включая клетки гемопоэтической системы. Признано его участие в развитии феномена МЛУ при раке легкого, толстой кишки, молочной железы, мочевого пузыря и простаты, а также при лейкозах. Данные о частоте экспрессии и функциональной значимости белка MRP при ОМЛ весьма противоречивы. По данным D.C. Zhou и соавт. [16], проанализировавших бластные клетки 91 первичного больного ОМЛ, экспрессия MRP1 наблюдалась у 24% пациентов, полные ремиссии в данной группе были достигнуты у 22% по сравнению с 84% в группе пациентов без экспрессии MRP1. M. Filipits и соавт. [17] определяли экспрессию MRP у 121 первичного больного ОМЛ, обнаружив при этом низкий уровень экспрессии у 30% пациентов, средний и высокий – у 46 и 24% соответственно. Экспрессия MRP1 не зависела от классических факторов прогноза (включая цитогенетические аномалии) и не влияла на непосредственные результаты лечения. Показана тенденция к снижению общей выживаемости в группе с высоким и средним уровнем экспрессии MRP1 [17]. В исследовании M. Schiach и соавт. [18] при анализе данных 331 больного показано, что в отличие от Pgp, оказывавшего влияние на непосредственные результаты лечения и общую выживаемость, экспрессия MRP1 является независимым фактором прогноза для безрецидивной выживаемости. Интересные данные опубликованы в 1996 г. B.J. Kuss и соавт. [19], которые, основываясь на локализации гена MRP1 на хромосоме 16, предположили, что дезактивация этого гена при специфической мутации (inv16), характерной для М4 ФАБ-варианта ОМЛ с эозинофилией, является причиной благоприятного прогноза при данном варианте заболевания. Был проведен анализ 22 больных с inv 16, у 5 из них была обнаружена делеция гена MRP, у этих больных отмечены достоверно лучшие показатели выживаемости [19].
Некоторые исследователи высказали предположение, что феномен МЛУ в большей степени связан с коэкспрессией нескольких белковых молекул. Так, O. Legrand и соавт. [12], проанализировав данные 132 больных, показали прогностическое значение одновременного обнаружения Pgp и MRP1 в бластных клетках при ОМЛ.
Активные исследования семейства АВС-транспортеров позволили в 1998 г. группе исследователей под руководством L.A. Doyle [20] выделить из клеточной линии рака молочной железы MCF-7/AdrVp, резистентной к даунорубицину, топотекану и митоксантрону, новый белок этого семейства. Он был назван «белком устойчивости рака молочной железы» (breast cancer resistance protein, BCRP) и отнесен к подсемейству G (ген ABCG2). Было показано, что перенос этого гена в химиочувствительные клеточные линии индуцирует резистентность к вышеуказанным препаратам при сохранении чувствительности к цисплатину, паклитакселу и винкаалкалоидам. Почти одновременно этот белок был выделен в двух других лабораториях, в связи с чем в литературе встречаются синонимичные обозначения MXR (mitoxantrone resistance protein) и ABCP (placental ABC transporter). Ген, кодирующий белок, располагается на длинном плече хромосомы 4 (4q22).
Хорошо известно, что антрациклины являются базисными препаратами при лечении ОМЛ, в связи с чем значение белка BCRP при ОМЛ начало активно изучаться сразу после его открытия. Данные продолжают накапливаться. Например, в исследовании Z. Benderra и соавт. [21] (149 первичных больных ОМЛ), завершенном в 2004 г., экспрессия белка BCRP обнаружена в 52%. В данной группе частота достижения полных ремиссий составила 43% против 69% в группе BCRP-отрицательных пациентов (р=0,005). Значимой корреляции между экспрессией BCRP и Pgp обнаружено не было. Исследователи делают вывод о том, что наихудший прогноз отмечен в группе больных, бластные клетки которых экспрессировали одновременно BCRP и Pgp (45% полных ремиссий в сравнении с 90% в группе без экспрессии обоих маркеров) [21]. Этот вывод был дополнен в более поздней работе той же исследовательской группы. У 81 больного ОМЛ была определена экспрессия MRP, BCRP и Pgp и продемонстрированы достоверно лучшие показатели общей выживаемости у пациентов, в бластных клетках которых белков МЛУ не обнаружено вообще либо обнаружен 1 белок.
В 2006 г. были опубликованы результаты работы итальянской группы исследователей [13], в которую были включены 73 первичных больных ОМЛ. Экспрессия BCRP выявлена у 33% больных, причем статистически значимых различий в достижении полной ремиссии у BCRP-позитивных и BCRP-негативных больных обнаружено не было. Тем не менее, в группе BCRP-позитивных пациентов отмечена достоверно более высокая частота рецидивов (78% против 38%), причем все рецидивы были ранними. В работе вновь подчеркивается важность комплексного исследования фенотипа МЛУ.
Несмотря на отчетливую связь BCRP с транспортом антрациклинов in vitro, до последнего времени не было продемонстрировано преимуществ ни одного из них (даунорубицин, идарубицин, митоксантрон) для преодоления резистентности опухолевых клеток, обусловленной этим белком. Тем не менее в 2002 г. B.L. Abbott с соавт. [22] in vitro показали значение BCRP в развитии резистентности к митоксантрону и топотекану при сохранении чувствительности к идарубицину. Необходимо отметить тот факт, что ни в одном исследовании не было показано статистически значимой связи экспрессии BCRP с классическими неблагоприятными факторами прогноза, в том числе с цитогенетическими аномалиями, что позволяет считать данный белок независимым прогностическим фактором. Помимо вышеописанных белков из семейства АВС-транспортеров, в развитии феномена МЛУ участвует еще ряд факторов. В 1993 г. при помощи моноклонального антитела LRP56 в полирезистентной Pgp-отрицательной клеточной линии рака легкого был выделен белок с молекулярной массой 110 кД, названный белком устойчивости рака легкого – LRP (lung resistance protein). Ген LRP, расположенный на хромосоме 16 в регионе, близком к гену MRP1, является гомологом главного везикулярного белка крыс. Исследования показали, что в отличие от АВС-белков он локализован не на клеточной мембране, а в цитоплазме и ассоциирован с везикулами и лизосомами, что позволяет считать его участником ядерно-цитоплазматического транспорта. Везикулы представляют собой расположенные в цитоплазме частицы, состоящие из РНК и белка. При культивировании клеток, экспрессирующих LRP, с антрациклинами эти препараты обнаруживаются внутри везикул и выводятся из клетки путем экзоцитоза. Гиперэкспрессия LRP в норме наблюдается в тканях толстой кишки, легкого, проксимальных почечных канальцев, коре надпочечников и макрофагов, однако его физиологические функции остаются неизвестными. Белок LRP обнаруживается в клетках различных злокачественных опухолей при отсутствии экспрессии Pgp и MRP1, что аассоциируется с резистентностью к доксорубицину, винкристину, цисплатину и мелфалану.
Первые данные о значении LRP при ОМЛ появились в 1996 г. Группа исследователей под руководством A.F. List [23] на достаточно разнородной группе из 86 больных (первичный и вторичный ОМЛ, РАИБ-Т, бластный криз хронического миелобластного лейкоза) показала, что у LRP-отрицательных пациентов частота достижения полной ремиии достоверно выше (35% против 68%). Была выявлена зависимость экспрессии LRP от возраста (старше 55 лет), подтвержденная во всех последующих исследованиях. В других исследованиях была продемонстрирована взаимосвязь экспрессии LRP с лейкоцитозом. Влияние экспрессии LRP на непосредственные результаты терапии отображено в табл. 2.
Таблица 2. Влияние экспрессии LRP на частоту достижения полной ремиссии (в %).
| Исследование | Экспрессия LRP1 у всех больных % | Полные ремиссии | |
| в группе Pgp+ | в группе Pgp- | ||
| R. Pirker и соавт. [24] | 36 | 55 | 72 |
| M. Filipits и соавт. [25] | 35 | 55 | 81 |
| M. Schaich и соавт. [18] | 40 | 68 | 80 |
Ряд исследователей, например M. Schaich и соавт. [18], на больших группах больных (n=331) показывают отсутствие самостоятельного значения экспрессии LRP как прогностического фактора. Неоднозначность данных и достаточно большой накопленный материал привели к тому, что в последние годы большинство исследователей, занимающихся проблемой лекарственной устойчивости, оценивают комплексный фенотип МЛУ, т.е. экспрессию двух и более белков и влияние на исход лечения их ассоциаций. Например, H.J. Huh и соавт. [26] в 2006 г., проанализировав данные 81 больного, показали прогностическую значимость коэкспрессии MRP и MDR1, а также MRP и LRP для 2-летней выживаемости, подтвердив тем самым выводы ряда предшествовавших исследований. В последних работах показано, что у больных, бластные клетки которых экспрессируют 3 и более маркера МЛУ, шанс достижения полной ремиссии при применении стандартных методов лечения чрезвычайно мал.
Отделением химиотерапии гемобластозов РОНЦ РАМН совместно с лабораторией генетики опухолевых клеток НИИ Канцерогенеза РОНЦ РАМН впервые в России проводится комплексное исследование фенотипа МЛУ у первичных больных ОМЛ (кроме М3), изучение его влияния на частоту достижения полной ремиссии, а также на возможность преодоления неблагоприятного фенотипа при использовании различных антрациклинов в схемах индукционной химиотерапии. Мы определяли экспрессию гена MDR1, белков BCRP, LRP и MRP1 в бластных клетках костного мозга в первый острый период, а также во время рецидива. На настоящий момент в исследование включены 30 больных – 18 (58%) мужчин и 12 (42%) женщин с различными ФАБ-вариантами ОМЛ (табл. 3).
Таблица 3. Распределение больных по ФАБ-вариантам
| ФАБ-вариант | Число больных | |
| абс. | % | |
| М1 | 8 | 26,7 |
| М2 | 8 | 26,7 |
| М4 | 7 | 23,3 |
| М4эоз | 1 | 3,3 |
| М5 | 4 | 13,3 |
| М6 | 2 | 6,7 |
Средний возраст пациентов составил 39,5 года (разброс 15–80 лет). У 22 больных перед началом лечения выполнено цитогенетическое исследование, в соответствии с которым больные были разделены на 3 прогностические группы (табл. 4).
Таблица 4. Распределение больных по прогностическим группам в зависимости от цитогенетических аномалий
| Прогноз | Число больных | |
| абс. | % | |
| Благоприятный | 4 | 18,2 |
| Промежуточный | 11 | 50 |
| Неблагоприятный | 7 | 31,8 |
У 22 больных проведено иммунофенотипическое исследование бластных клеток, причем у 76% выявлена экспрессия CD34.
Таким образом, число больных с неблагоприятными цитогенетическими и иммунологическими признаками было сравнительно выше, чем в среднем среди больных с ОНЛЛ. 23 больных получали лечение по протоколу РОНЦ для ОМЛ, включающее индукцию ремиссии по стандартной схеме 3+7+7 с этопозидом и идарубицином, консолидацию ремиссии высокими дозами цитозара (курсовая доза 18 г/м2) в комбинации с идарубицином (2 курса), поддерживающую терапию по схеме 1+5+5 также с идарубицином и этопозидом (4–6 курсов). По нашим данным, частота достижения полной ремиссии при подобной программе лечения составляет 72%, причем у всех больных с ремиссиями костномозговые ремиссии достигнуты после 1-го курса химиотерапии. Прочие пациенты получали индукционную химиотерапию по схеме 3+7 с даунорубицином в дозе 45 мг/м2. В целом полные ремиссии были достигнуты у 20 (66,7%) больных, 10 (33,3%) пациентов оказались резистентными к проводимому лечению. Резистентными считались пациенты, у которых ремиссия не была получена после 2 курсов стандартной химиотерапии. У всех пациентов проводился забор костного мозга перед началом лечения, образцы костного мозга в пробирках с ЭДТА доставлялись в лабораторию, где в течение 24 ч с момента взятия материала оценивали экспрессию белков МЛУ в реакции с моноклональными мышиными антителами фирмы CHEMICON: к MRP1 – MAB 4122, к LRP – MAB4126, к BCRP – MAB4146, к MDR1 – UIC2. Анализ экспрессии проводился методом проточной лазерной флуорометрии на приборе FACScan Becton Dickinson. Экспрессия белка считалась положительной при его обнаружении более чем в 25% бластных клеток. Положительная экспрессия Pgp вывлена у 64,3% больных, MRP1 – у 46,4%, LRP – у 64,3%, BCRP – у 42,9%. Эти данные несколько превышают мировые, что может быть объяснено как относительно небольшой выборкой больных, так и совокупностью неблагоприятных факторов прогноза.
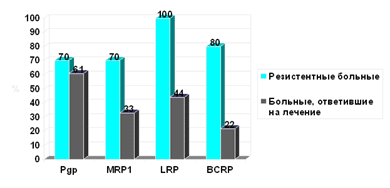
Рис. 2. Экспрессия белков МЛУ в группе больных, ответивших на лечение, и у резистентных больных
В группе резистентных больных отмечается более высокая экспрессия белков МЛУ, причем для ВСRР и LRP различия достоверны (р=0,002; рис. 2). Частота достижения полной ремиссии оказалась ниже при экспрессии любого из изучаемых белков, причем вновь для BCRP и LRP различия были статистически достоверны (р=0,004; рис. 3).
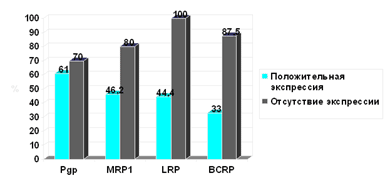
Рис. 3. Частота достижения полной ремиссии в зависимости от экспрессии белков МЛУ
В исследованной группе у всех больных выявлена экспрессия хотя бы одного белка МЛУ. Мы оценивали влияние числа экспрессированных маркеров МЛУ на процент достижения полных ремиссий. Лишь у 40% больных обнаружен только 1 АВС-белок, у большинства больных обнаружено 2 белка и более (табл. 5).
Таблица 5. Распределение пациентов в зависимости от числа экспрессируемых маркеров
| Число экспрессируемых маркеров | Число больных | |
| абс. | % | |
| 1 | 12 | 40,0 |
| 2 | 7 | 23,3 |
| 3 | 6 | 20,0 |
| 4 | 5 | 16,7 |
Из полученных нами данных следует, что бластные клетки всех больных, не ответивших на терапию, экспрессировали более одного маркера МЛУ, у 80% резистентных больных отмечена экспрессия трех и четырех маркеров, в то время как в группе чувствительных больных 1–2 маркера экспрессировались бластными клетками у 83% пациентов (рис. 4).
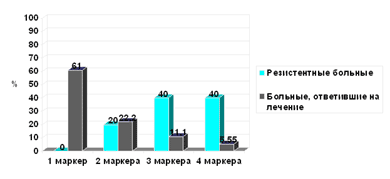
Рис. 4. Зависимость достижения полной ремиссии от числа экспрессируемых белков МЛУ
Более того, необходимо отметить, что у единственного больного, ответившего на лечение и экспрессировавшего все 4 белка (более 50% бластных клеток), развился ранний рецидив. Определенный интерес представляет зависимость экспрессии белков МЛУ от цитогенетической прогностической группы. Несмотря на то что в ряде исследований подобная связь отрицается, по нашим данным, у всех больных из группы с неблагоприятными цитогенетическими аномалиями бластные клетки экспрессировали более двух маркеров МЛУ.
Заключение
В связи с потенциальной курабельностью ОМЛ феномен МЛУ и пути его преодоления вызывают большой интерес исследователей во всем мире. Данные о прогностической значимости ранее известных и вновь открываемых факторов продолжают накапливаться и все еще остаются весьма неоднозначными. Ряд исследователей полностью отвергают значение описанных белковых субстанций как фактора прогноза, другие же считают необходимым ввести обследование фенотипа МЛУ в рутинную практику. Наши данные показывают, что наличие экспрессии одного белка МЛУ не является прогностически неблагоприятным признаком в условиях современной терапии, экспрессия более двух белков остается прогностически неблагоприятной.
Материал взят из журнала "Онкогематология", №1-2, 2006.
Литература
1. Савченко В.Г., Паровичникова Е.Н. Лечение острых лейкозов. М., 2004.
2. Ставровская А.А. Резистентность больных гемобластозами к лекарственной терапии. В кн.: Клиническая онкогематология. Под ред. М.А. Волковой. М., Медицина; 2001.
3. Gregory D.L., Tito F., Susan E.B. The role of ABC transporters in clinical practice. The Oncologist 2003; 8(5):411–24.
4. Dean M., Rzhetsky A., Allikmets R. The human ATP-binding cassette (ABC) transporter superfamily. Genome Res 2001;11(7):1156–66.
5. Riordan J.R., Ling V. Purification of P-glycoprotein from plasma membrane vesicles of Chinese hamster ovary cell mutants with reduced colchicine permeability. J Biol Chem 1979;254(24):12701–5.
6. Guerci A., Merlin J.L., Missoum N. et al. Predictive value for treatment outcome in acute myeloid leukemia of cellular daunorubicin accumulation and P-glycoprotein expression simultaneously determined by flow cytometry. Blood 1995;85: 2147–53.
7. van der Kolk D.M., de Vries E.G., van Putten W.J. et al. P-glycoprotein and multidrug resistance protein activities in relation to treatment outcome in acute myeloid leukemia. Clin Cancer Res 2000;6:3205–14.
8. Marie J.P., Legrand O. MDR1/P-GP expression as a prognostic factor in acute leukemias. Adv Exp Med Biol 1999;457:1–9.
9. Leith C.P., Kopecky K.J., I-Ming Chen et al. Frequency and clinical significance of the expression of the multidrug resistance proteins MDR1/P-glycoprotein, MRP1, and LRP in acute myeloid leukemia. A Southwest Oncology Group Study. Blood 1999;94(3): 1086–99.
10. Benderra Z., Faussat A.M., Sayadaуе L. et al. MRP3, BCRP, and P-glycoprotein activities are prognostic factors in adult acute myeloid leukemia. Clin Cancer Res 2005;11:7764–72.
11. van Stijn A., van der Pol M.A., Kok A. et al. Differences between the CD34+ and CD34- blast compartments in apoptosis resistance in acute myeloid leukemia. Haematologica 2003;88(5):497–508.
12. Legrand O., Zompi S., Perrot J.Y. et al. P-glycoprotein and multidrug resistance associated protein-1 activity in 132 acute myeloid leukemias according to FAB subtypes and cytogenetics risk groups. Haematologica 2004;89(1):34–41.
13. Damiani D., Tiribelli M., Calistri E. et al. The prognostic value of P-glycoprotein (ABCB) and breast cancer resistance protein (ABCG2) in adults with de novo acute myeloid leukemia with normal karyotype. Haematologica 2006;91:825–8.
14. Hunter H.M., Pallis M., Seedhouse C.H. et al. The expression of P-glycoprotein in AML cells with FLT3 internal tandem duplications is associated with reduced apoptosis in response to FLT3 inhibitors. Br J Hemat 2004;127(1):26–33.
15. Cole S.P., Bhardwaj G., Gerlach J.H. et al. Overexpression of a transporter gene in a multidrug-resistant human lung cancer cell line. Science 1992;258(5088):1650–4.
16. Zhou D.C., Zittoun R., Marie J.P. Expression of multidrug resistance-associated protein (MRP) and multidrug resistance (MDR1) genes in acute myeloid leukemia. Leukemia. 1995;9(10):1661–6.
17. Filipits M., Stranzl T., Pohl G. et al. MRP expression in acute myeloid leukemia. An update. Adv Exp Med Biol 1999;457:141–50.
18. Schaich M., Soucek S., Thiede Ch. et al. MDR1 and MRP1 gene expression are independent predictors for treatment outcome in adult acute myeloid leukaemia. Br J Hemat 2005;128(3):324–32.
19. Kuss B.J., Deeley R.G., Cole S.P. et al. The biological significance of the multidrug resistance gene MRP in inversion 16 leukemias. Leuk Lymphoma 1996;20(5–6):357–64.
20. Doyle L.A., Yang W., Abruzzo L.V. et al. A multidrug resistance transporter from human MCF-7 breast cancer cells. Proc Natl Acad Sci 1998;95:15665–70.
21. Benderra Z., Faussat A.-M., Sayada L. et al. Breast cancer resistance protein and P-glycoprotein in 149 adult acute myeloid leukemias. Clin Cancer Res 2004;10:7896–902.
22. Abbott B.L., Colapietro A.-M., Barnes Y. et al. Low levels of ABCG2 expression in adult AML blast samples. Blood 2002;100(13):4594–601.
23. List A.F., Spier C.S., Grogan T.M. et al. Overexpression of the major vault transporter protein lung-resistance protein predicts treatment outcome in acute myeloid leukemia. Blood 1996;87(6):2464–9.
24. Pirker R., Pohl G., Stranzl T. et al. The lung resistance protein (LRP) predicts poor outcome in acute myeloid leukemia. Adv Exp Med Biol 1999;457:133–9.
25. Filipits M., Pohl G., Stranzl Th. et al. Expression of the lung resistance protein predicts poor outcome in de novo acute myeloid leukemia. Blood 1998;91(5): 1508–13.
26. Huh H.J., Park C.J., Jang S. et al. Prognostic significance of multidrug resistance gene 1 (MDR1), multidrug resistance-related protein (MRP) and lung resistance protein (LRP) mRNA expression in acute leukemia. J Korean Med Sci 2006;21(2):253–8.



