В.Ф. Семиглазов, В.В. Семиглазов, А.Е. Клецель, Е.К. Жильцова,
В.Г. Иванов, А.А. Божок, Р.В. Донских, С.Г. Петровский, Р.М. Палтуев,
Г.А. Дашян, К.Ю. Зернов, А.В. Ефименко, И.А. Кочетова
НИИ онкологии им. проф. Н.Н. Петрова, Санкт-Петербург, Россия
Хотя неоадъювантное системное лечение РМЖ имеет уже 15-летнюю историю, оно пока не вошло в стандарт лечения этих опухолей. Достаточно сказать, что в мире имеется лишь 6 опубликованных рандомизированных испытаний неоадъювантной химиотерапии и четыре рандомизированных испытания неоадъювантной гормонотерапии (два с участием НИИ онкологии им.проф. Н.Н.Петрова). Многие врачи, опираясь на "персональный опыт" полагают, что неоадъювантная химиотерапия эффективнее и безопаснее гормонотерапии, т.к. позволяет в относительно короткие сроки (9-12 недель) добиться заметного регресса опухоли для выполнения хирургического этапа (от мастэктомии до органосохраняющей операции в зависимости от остаточного размера опухоли).
В последние годы - в связи с большим вниманием к сохранным методам хирургического вмешательства, а также из-за накопления дополнительных данных о механизмах эстрогенозависимости РМЖ и гормонального канцерогенеза, все чаще делаются попытки проведения неоадъювантной гормонотерапии рака молочной железы, прежде всего, на основе применения антиэстрогенов и ингибиторов ароматазы. Неоадъювантная терапия рассматривается, прежде всего, как уникальная модель тестирования активности нового терапевтического подхода или как способ определения потенциального значения биологических факторов в оценке дальнейшего клинического течения и исхода заболевания. В этих случаях больные РМЖ получают лечение de novo; результаты оцениваются быстро и вся перечисленная информация получается на относительно небольшом числе пациентов и в кратчайшие сроки, исчисляемыми месяцами, а не годами (как при проведении адъювантной терапии). К преимуществам неоадъювантного лекарственного лечения относят следующие моменты: воздействие на микрометастазы; уменьшение массы опухоли и уменьшение объема выполнения оперативного этапа (до функционально выгодных и органосохранных вариантов); определение индивидуальной чувствитель-ности опухоли к использованным противоопухолевым агентам. Клиническая регрессия опухоли коррелирует со степенью терапевтического патоморфоза в опухолях и является важным прогно-стическим фактором, отражающим чувствительность опухоли к проводимой терапии. Важность данного факта состоит в том, что позволяет в случаях резистентности опухоли определить оптимальный подход в назначении адъювантного лечения. Эффективность предоперационной терапии может служить одним из критериев прогноза при местнораспространенном РМЖ. При выраженном клиническом эффекте рецидивы и метастазы возникают реже и сроки их появления удлиняются.
В НИИ онкологии с 1997 по 2004г. было проведено четыре рандомизированных испытаний неоадъювантной эндокринотерапии РМЖ. Первое из них выполнено в рамках Международного многоцентрового протокола 024 "Неоадъювантная гормонотерапия летрозолом против тамоксифена у женщин с РМЖ ЭР+/ПР+ в постменопаузе" (спонсор компания "Новартис" (Швейцария)).
Результаты исследования 024, включавшего 377 больных ЭР+ доказали что частота клинических ответов значительно выше при лечении летрозолом, в сравнении с тамоксифеном (55% против 36%; Р<0,001) [табл.1]. Пациентам, получавшим летрозол, значительно чаще выполнялась органосохраняю-щие операции, чем в группе "тамоксифена" (45% против 35%; Р=0,022). Медиана времени до появления ответа равнялась 66 дням в группе "летрозол" и 70 дням в группе "тамоксифен".
Таблица 1. Сравнительная эффективность фемары и тамоксифена в неоадъювантной терапии
|
Методы оценки эффекта гормонотерапии |
Фемара (154 больных) |
Тамоксифен (170 больных) |
Значение Р |
|---|---|---|---|
|
Клиническая оценка (пальпация) - Объективный ответ - Полный регресс - Частичный регресс |
55% 10% 45% |
36% 4% 32% |
<0.001 |
|
Ультразвуковая оценка - Объективный ответ - Полный регресс - Частичный регресс |
35% 3% 32% |
25% 1% 24% |
0.042 |
|
Маммографическая оценка - Объективный ответ - Полный регресс - Частичный регресс |
34% 4% 30% |
16% 0% 16% |
<0.001 |
|
Органосохраняющие операции |
45% |
35% |
0.022 |
Особенно высокие отличия в пользу летрозола наблюдались у больных, опухоли которых экспрессировали одновременно HER1 и/или HER2 и рецепторы эстрогенов (ЭР+). Найденная закономерность подтверждается и другими исследованиями об относительно слабом ответа таких опухолей на терапию тамоксифеном, что близко по сути к механизму прогрессии на тамоксифене из-за его преобладающего эффекта агониста в присутствии НЕR1 или 2 или при активации HER1 или 2 - патогенетического механизма роста РМЖ.
Второе клиническое испытание походило по характеру рандомизации и используемым препаратам на Международный адъювантный проект АТАС, только со значительно меньшим числом включенных пациентов "Аримидекс (А) против тамоксифена (Т) против комбинации (А+Т) в неоадъювантной эндокринотерапии постменопаузальных больных РМЖ с ЭР+ опухолями".
Таблица 2. Величина ответа опухоли на различные виды неоадъювантной эндокринотерапии постменопаузальных больных РМЖ (ЭР+/ПР+)
|
Неоадъювантная эндокринотерапия |
Объективный ответ |
Стабилизация |
Прогрессирование |
|
|---|---|---|---|---|
|
Полный |
Частичный* |
|||
|
Аримидекс |
13,3% |
80% |
6,6% |
0 |
|
Аримидекс + Тамоксифен |
0 |
42,8% |
57,1% |
14,2% |
|
Тамоксифен |
10,3% |
48,2% |
37,1% |
3,4% |
С 1998 г по 2002 г. в исследование включено 87 больных РМЖ постменопаузального возраста (от 55 до 74 лет) с рецептор-положительными опухолями (ЭР+ и/или ПР+), отнесенными к категории Т
Дизайн исследования и схема рандомизации представлены на рис.1.
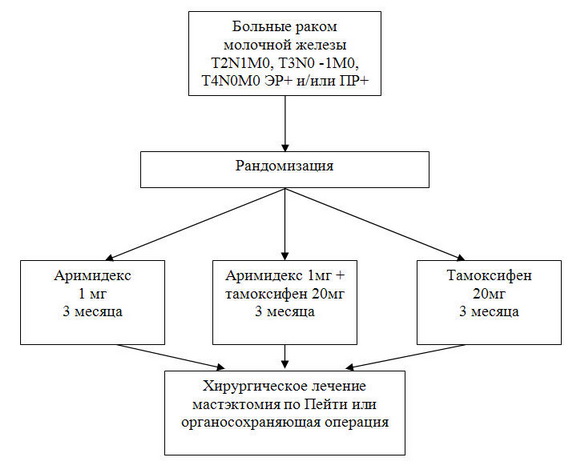
Рис. 1. Дизайн клинических испытаний неоадъювантной эндокринотерапии в НИИ онкологии им.проф. Н.Н.Петрова.
Основной целью исследования было сравнение величины объективных ответов опухоли на лечение (частичный или полный регресс опухоли) определяемый с помощью клинического метода (пальпация), рентгеномаммографии и ультразвукового исследования (до начала и после окончания неоадъювантной эндокринотерапии). Одной из целей исследования было также определение частоты выполнения органосохраняющих операций в различных лечебных группах.
Для оценки величины ответа опухоли на лечение в работе использованы стандартные критерии ВОЗ с двухмерным измерением наибольших диаметров.
Полный ответ (регресс) - 100% исчезновение опухоли
Частичный ответ - уменьшение размера на 50% и более.
Стабилизация - уменьшение размера опухоли менее чем на 50%.
Прогрессирование - увеличение размера опухоли более чем на 25%.
При клинической оценке (пальпация) полный ответ опухоли наблюдался у 13,3% больных 1-й группы (получавших лечение аримидексом), 10,3% больных 3-й группы (получавших тамоксифен) и ни разу во 2-й группе (получавших комбинированное лечение аримидексом и тамоксифеном (табл.1). Частичный ответ достоверно чаще наблюдался в группе больных, получавших один аримидекс по сравнению с леченными тамоксифеном или получавшими комбинированное лечение (тамоксифен + аримидекс) (80% против 48% против 42%, Р=0,048). При оценке лечебного эффекта с помощью маммографии объективный ответ (частичный или полный регресс опухоли) наблюдался у 55,5% больных, получавших аримидекс, 40% больных, получавших комбинированное лечение (А+Т) и 36% больных, получавших тамоксифен (Р=0,058). При изучении лечебного эффекта с помощью динамического ультразвукового исследования молочных желез объективный ответ зарегистрирован у 44% больных, получавших аримидекс, 32% больных, получавших комбинированную эндокринотерапию (А+Т) и 30% больных, получавших один тамоксифен.
При патоморфологическом изучении операционных препаратов полное исчезновение инвазивных опухолевых клеток (РСР) наблюдалось у двух больных после лечения аримидексом, одной больной - после комбинированного лечения и у одной больной - после терапии тамоксифеном.
Органосохраняющие операции (сегментарная резекция + подмышечная диссекция) были выполнены у 42% больных 1-й группы (получавших один аримидекс), у 30% больных, получавших комбинированную эндокринотерапию (А+Т) и 30% больных, получавших один тамоксифен, р=0,056.
Ответ на любой вид неоадъювантной эндокринотерапии оказался наиболее высоким и значимым при высоком уровне экспресс рецепторов эстрогенов. В работе было также показано явное уменьшение уровня рецепторов прогестерона (РП) в группе больных, получавших один аримидекс. У 14 из 30 больных получавших тамоксифен (т.е. в 46,6% случаев) после лечения не определялись рецепторы прогестерона. Средний уровень рецепторов прогестерона до лечения аримидексом достигал 106 fmol/mg, а после окончания лечения - лишь 11,3 fmol/mg. Экспрессия РП эффективно подавлялась аримидексом, но не тамоксифеном.
Любой вариант эндокринотерапии легко переносился пациентами. Наиболее частым побочным эффектом лечения оказались приливы, встретившиеся соответственно по группам в 21%, 24%, 25% случаев (р>0,5). При наблюдении за больными в течение 38 месяцев не отмечалось смертельных исходов из-за осложнений лечения.
В клиническое испытание "Неоадъювантная эндокринотерапия экземестаном (аромазином) против тамоксифена" с 1997 г по 2004 г вошли 127 больных PMЖ T
Вторичной целью исследования было определение частоты выполнения органосохраняющих операций в различных лечебных группах.
Как видно из таблицы 3 предоперационная (неоадъювантная) терапия экземестаном (аромазином) оказалась значительно более эффективной, чем лечение тамоксифеном. При клинической оценке величина общего объективного ответа опухоли на терапию аромазином оказалась почти в два раза выше, чем на лечение тамоксифеном (90.5% против 48.4%, Р=0.049). При рентгеномаммографической оценке абсолютные показатели ниже, чем при клинической оценке, но тенденция превосходства аромазина над тамоксифеном сохраняется, особенно по частоте частичного ответа опухоли (58% против 20%).
Число больных с прогрессированием заболевания во время эндокринотерапии оказалось выше в группе "тамоксифен" (10% против 3.4%, P=0.076) [табл. 4]. Важным критерием эффективности неоадъювантного лечения оказалась частота выполнения органосохраняющих операций у больных, которым до неоадъювантной эндокринотерапии планировалась радикальная мастэктомия. После завершения предоперационного лечения органосохраняющие операции (сегментарная резекция, квадрантэктомия + подмышечная диссекция) выполнены у 31,6% больных, получавших лечение экземестаном, и у 13.3% больных, леченных тамоксифеном (Р=0.048).
Таблица 3. Клиническая оценка величины ответа опухоли на неоадъювантную эндокринотерапию экземестаном (аромазином) против тамоксифена у постменопаузальных больных РМЖ с ЭР+/ПР+ опухолями (НИИ онкологии им. проф. Н.Н.Петрова, 1997-2004)
|
Вид неоадъювантной эндокринотерапии |
Клинический ответ |
||
|---|---|---|---|
|
полный |
частичный |
Общий объективный ответ |
|
|
Тамоксифен |
9.7% |
38.7% |
48.4% |
|
Экземестан |
4.8% |
85.7% |
90.5% |
|
Значение Р |
0.098 |
0.046 |
0.049 |
Таблица 4. Маммографическая оценка величины ответа опухоли на неоадъювантную эндокринотерапию экземестаном (аромазином) против тамоксифена у постменопаузальных больных РМЖ с ЭР+/ПР+ РМЖ (НИИ онкологии им. проф. Н.Н.Петрова, 1997-2004)
|
Вид неоадъювантной эндокринотерапии |
Маммографический ответ |
|||
|---|---|---|---|---|
|
полный |
частичный |
стабилизация |
прогрессирование |
|
|
Тамоксифен |
3.3% |
20% |
66.6% |
10% |
|
Экземестан |
6.8% |
58% |
38.5 |
3.4% |
|
Значение Р |
0.088 |
0.049 |
0.056 |
0.076 |
К настоящему времени опубликованы результаты шести рандомизированных испытаний первичной химиотерапии и четырех испытаний (два с участием НИИ онкологии им. проф. Н.Н.Петрова) первичной эндокринотерапии. Из этих и других нерандомизированных исследований выяснилось, что эффективность неоадъювантной химиотерапии в постменопаузе значительно ниже при рецептор-положительных опухолях в сравнении с рецептор-отрицательными (ЭР-/ПР-) опухолями. Однако прямого рандомизированного сравнения эффективности неоадъювантной химиотерапии и эндокринотерапии у постменопаузальных больных РМЖ с рецептор-положительными (ЭР+ и/или ПР+) опухолями до нашего исследования не проводилось. В НИИ онкологии им. проф. Н.Н.Петрова в 1998 г начато специальное исследование сравнительной эффективности неоадъювантной (предоперационной) эндокринотерапии (аромазин или аримидекс) и химиотерапии (схема AT – доксорубицин + таксол). С марта 1998 г по июнь 2004 г в исследование вошли 152 "постменопаузальных" больных РМЖ с ЭР+ и/или ПР+ опухолями Т
Таблица 5. Клиническая оценка величины ответа опухоли на неоадъювантную терапию у постменопаузальных больных с ЭР+/ПР+ опухолями. (НИИ онкологии 1998-2004)
|
Вид неоадъювантной терапии |
Объективный общий ответ (%) |
Органосохраняющие операции (%) |
|---|---|---|
|
Химиотерапия по схеме А+Т* |
75.6% |
24.3% |
|
анастразол |
75.0% |
34.0% |
|
экземестан |
78.9% |
34.2% |
*А+Т – доксорубицин + таксол
Как видно из таблицы 5 величина общего объективного ответа на ингибиторы ароматазы и на неоадъювантную химиотерапию статистически не отличалась (аромазин - 78.9%, аримидекс - 75%, химиотерапия AT - 75,6%). Имелась очевидная тенденция более частого выполнения органосохраняющих операций в группе больных с неоадъювантной эндокринотерапией в сравнении с химиотерапией (34.2% против 24.3%, Р= .058). Показатели трехлетней безрецидивной выживаемости достоверно не отличались: 80.2% - в "химиотерапевтической" группе и 78,6% - в "эндокринной" группе. В группе больных, получавших неоадъювантную химиотерапию, наиболее частыми побочными токсическим эффектами lll/lV степени были: алопеция (79.3%), нейтропения (43,1%), нейропатия (30%), кардиотоксичность (6.8%). Эндокринотерапия переносилась хорошо (приливы - 23%, редкие случаи арталгии - 6%). Таким образом, впервые было показано, что неоадъювантная эндокринотерапия (аромазин, аримидекс) не уступает первичной химиотерапии (схема AT) по величине объективных ответов на лечение, но значительно легче переносится пациентами. Поэтому предоперационная эндокринотерапия антиароматазными препаратами может быть альтернативой химиотерапии у пожилых больных с ЭР+/ПР+ опухолями.
Российский проект по неоадъювантной системной терапии (первичная эндокринотерапия против химиотерапии) привлек внимание крупнейших форумов мира: его результаты заслушаны в 2004 г на Конгрессе по противораковой терапии в Париже, на Ш Международной конференции по раку молочной железы в Гамбурге, на пленарном заседании Американского общества клинической онкологии (ASCO) в Новом Орлеане (2004), на 5-й конференции по раку молочной железы в Нцце (2006).
Последние исследования ясно продемонстрировали, что ингибиторы ароматазы (аримидекс, фемара) и инактиватор ароматазы (экземестан) могут стать препаратами выбора для терапии первой линии гормоночувствительного метастатического РМЖ, а профиль безопасности препаратов делают привлекательным для назначения их в неоадъювантной и адъювантной терапии у постменопаузальных женщин с ЭР+/ПР+ опухолями. В перспективе они могут быть исследованы в качестве препаратов для "химиопрофилактики" рака молочной железы у женщин высокого риска.


