К.П. Лактионов, А.В. Кузнецов, А.С. Бурлаков
ГУ РОНЦ им. Н.Н. Блохина РАМН, Московская городская
онкологическая больница № 62
В статье представлены результаты реконструкции молочной железы ректо-абдоминальным лоскутом у 116 пациентов. У 32% больных в послеоперационном периоде были зафиксированы послеоперационные некротические изменения: лоскут 11,8%, донорская зона 8,4%, лоскут и донорская зона 11,8%. Анализ кровоснабжения и осложнений выявил среди 5 вариантов операций по восстановлению формы груди преимущество использования свободного TRAM (transversrectusabdominismyocutaneous)-лоскута и TRAM-лоскута на 2-х мышечных ножках. Ожирение, курение, неоадъювантная химиотерапия, проведённая в объёме 6 и более курсов менее, чем за 1 год до реконструкции, достоверно увеличивают количество послеоперационных некрозов лоскута и донорской зоны. Проведён анализ влияния местных факторов риска: лучевой терапии и рубцов после ранее произведённых операций на результаты реконструкции. Соблюдение правил подбора пациентов позволяет полностью исключить наличие глубоких послеоперационных некрозов и снизить количество поверхностных некрозов до 6,6% со стороны лоскута, до 4,4% со стороны донорской зоны.
This article represents the results of TRAM-flap breast reconstruction. The number of patients was 116. There were 3 types of postoperative necrosis: flap (11,8%), donor site (8,4%), flap+donor site (11,8%). Study of flap microcirculation and complication analysis revealed advantage of free TRAM-flap and bipedicled TRAM-flap among 5 types of reconstructive operations. Obesity, smoking and neoadjuvant chemotherapy (6 and more cycles) significantly increased number of postoperative flap and donor site necrosis. The analysis of influence of local risk factors (breast irradiation and previous operative scars) on the results of reconstruction was performed. Careful patients selection allows to prevent completely deep postoperative necrosis and decreases the number of superficial flap necrosis up to 6,6% and donor site – up to 4,4% .
В настоящее время восстановление формы груди после мастэктомии с использованием ректо-абдоминального лоскута стало стандартной операцией, которая выполняется во многих лечебных учреждениях [1-6]. Однако результаты проводимых реконструкций оставляют желать лучшего и дают, по оценкам различных авторов, от 13 до 20 % [6-7] послеоперационных некрозов лоскута, различной степени выраженности. При этом большинство авторов не указывает данные по количеству некрозов абдоминальной донорской области.
Настоящая работа была проведена с целью улучшения качества лечения и сокращения количества осложнений при операциях на молочной железе с использованием ректо-абдоминального лоскута. Нами проведён анализ 116 случаев использования 5 вариантов операций по реконструкции ректо-абдоминальным лоскутом у больных раком молочной железы в 3-х специализированных хирургических отделениях за 2002-2005г.
Наиболее часто в нашем исследовании применялись варианты свободного TRAM (transvers rectus abdominis myocutaneous)-лоскута (45%) и TRAM-лоскута на 2-х мышечных ножках (41%), значительно реже использовался лоскут на 1-ой мышечной ножке (9% случаев). Вертикальный ректо-абдоминальный лоскут использовался в 4% и вариант TRAM-лоскута на одной мышечной ножке с дополнительной васкуляризацией в 1% случаев. Большинство реконструкций (75%) было выполнено одномоментно с удалением молочной железы. Основной контингент наблюдений (77,6 %) составили женщины в наиболее трудоспособном и социально-активном возрасте от 30 до 49 лет. Основным видом опухоли у проанализированной нами группы пациентов со злокачественными новообразованиями молочной железы был инфильтративный рак (99%), протоковой формы в 46,1% случаев. Наибольшую группу (50%) составили больные со II стадией заболевания. У 65,5% пациенток перед восстановительным этапом была проведена противоопухолевая терапия в различном объёме.
Из 116 больных у 32% пациентов в послеоперационном периоде были зафиксированы послеоперационные некротические изменения. По локализации некрозов данные случаи могут быть разделены на три группы: пациентки с изолированным некрозом только в области лоскута 11,8%, с изолированным некрозом в области донорской зоны 8,4% и пациентки, имевшие сочетанные осложнения и на лоскуте и в абдоминальной донорской зоне 11,8%. Сочетание, как правило глубины некроза с обширностью поражения, позволило выделить две основные степени повреждения ткани: это поверхностные, краевые некрозы и глубокие обширные некрозы с тяжёлым длительным течением послеоперационного периода.
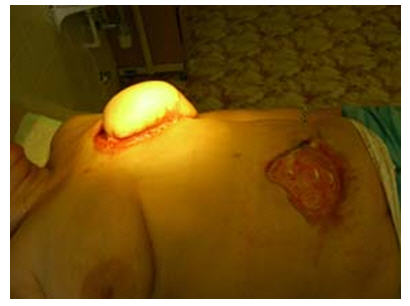
Рис. 1. Последствия глубоких некрозов в области лоскута и донорской зоны после реконструкции ректо-абдоминальным лоскутом.
Проведённая работа показала, что качество кровоснабжения и следовательно количество некрозов лоскута напрямую зависит от варианта операции таб.1.
Из трёх наиболее часто применяемых для восстановления формы груди вариантов ректо-абдоминального лоскута, наилучшее кровоснабжение и соответственно наименьшее количество осложнений (11,5%) имелось при варианте свободного TRAM -лоскута. Однако в одном случае возник полный липонекроз лоскута с частичным некрозом кожи, который был связан с тромбозом сосудистой ножки. В последствии этот лоскут был оперативно удалён, что говорит о возможности полной неудачи в случае нарушения проходимости сосудистой ножки при использовании варианта свободного ректо-абдоминального лоскута. Краевые зоны лоскута на двух мышечных ножках имели несколько худшее кровоснабжение и больший процент некрозов (33,3%). Но некрозов центральных зон не было выявлено ни в одном случае. Полного некроза лоскута так же не было ни в одном случае, что говорит о надёжности данного вида операции. Наибольшее количество осложнений имелось в группе больных с перемещением ректо-абдоминального лоскута на 1-ой мышечной ножке (50%).
Полученные данные говорят о предпочтительности использования с целью реконструкции молочной железы, при прочих равных условиях, свободного TRAM-лоскута и TRAM-лоскута на 2-х мышечных ножках. Учитывая, что вариант на одной мышечной ножке имеет наихудшее кровоснабжение, даже при незначительных признаках недостаточного кровоснабжения следует применять отсечение краевых зон или дополнительную васкуляризацию, в сомнительных случаях отдавая предпочтение вариантам операции по пересадке свободного лоскута и перемещению на двух мышечных ножках. В случае выявления признаков недостаточного кровообращения в краевых зонах лоскута на двух мышечных ножках или свободного лоскута так же можно порекомендовать отсечение этих областей с целью профилактики послеоперационных некрозов.
По ходу набора материала стало очевидно, что послеоперационные осложнения не всегда зависят от варианта операции. Статистически одинаковое количество осложнений в донорской зоне с разбросом от 19,2 до 22,9% (p>0,05) при всех 5 видах операции (таб.1) подтвердило факт независимости количества абдоминальных некрозов от варианта реконструкции. При глубоких некрозах в краевых зонах лоскута, имелось расхождение швов даже в центральной его части, где кожные края ишемизировались, швы прорезались, не только со стороны лоскута, но и со стороны ткани грудной стенки. В результате края раны расходились на 15 – 20 сутки. Это говорило о явном снижении способности к активной репарации и ткани трансплантата, и ткани грудной стенки. Из всех пациентов с некрозами, у 40% имелись совместные некрозы лоскута и донорской зоны. Выявленные факты определили дальнейший поиск возможных причин некротических изменений в послеоперационном периоде.
Для анализа были выделены предположительные предоперационные системные и местные факторы риска возникновения некрозов после восстановления молочной железы различными вариантами ректо-абдоминального лоскута. К системным факторам были отнесены: возраст, наличие ожирения, предоперационная противоопухолевая химиотерапия и курение, к местному фактору со стороны реципиентной зоны - лучевая терапия проведённая перед реконструктивной операцией, со стороны донорской зоны - наличие рубцов в абдоминальной области после ранее произведённых операций.
При сравнении результатов реконструкции молочной железы ректо-абдоминальным лоскутом у пациентов в возрасте 50 лет и старше (20 человек) с группой моложе 50 лет (96 больных) не было получено достоверно подтверждённых данных (p>0,05) об увеличении количества некрозов.
В ходе работы доказано, что курение достоверно (p<0,05) увеличивает у больных с реконструкцией количество некрозов не только лоскута в 2,4 раза, но и абдоминальной донорской зоны в 3,5 раза, по сравнению с не курящими пациентами [8].
При сравнительном анализе результатов реконструкции у 34 больных с наличием рубцов в донорской зоне с результатами полученными у 82 пациенток без рубцов в абдоминальной области не было найдено статистически достоверного различия в количестве осложнений (p>0,05). На основании этого можно сделать вывод о том, что наличие рубцов в донорской зоне не оказывает существенного влияния на результаты реконструкции молочной железы ректо-абдоминальным лоскутом. Однако, данное утверждение справедливо только при условии правильного выбора варианта реконструкции в связи с возможным изменением анатомии кровоснабжения донорской зоны TRAM–лоскута после предшествующих операций.
Для оценки влияния наличия ожирения на результаты операции было произведено исследование количества осложнений у больных с ожирением (индекс массы тела свыше 29,0 кг/м2) и у больных без ожирения (индекс массы тела 29,0 кг/м2 и менее). Кроме явного увеличения количества осложнений у больных с ожирением, в 3,0 раза по лоскуту (p<0,01) и в 2,5 раза по донорской зоне (p<0,05), обратил на себя внимание тот факт, что в группе с ожирением наблюдался сдвиг в сторону увеличения тяжести осложнений. И со стороны лоскута, и со стороны донорской зоны у больных с ожирением имелось большее количество глубоких некрозов, чем поверхностных.
Результаты исследования позволили говорить об отсутствии влияния проведённой до реконструкции лучевой терапии на состояние ректо-абдоминального лоскута. При сравнении количества некрозов лоскута в группах с лучевой терапией (40 больных) и без лучевой терапии (76 больных) не было получено достоверного различия (p>0,05). Очевидно, что на трансплантат, получающий независимое от реципиентной зоны кровоснабжение, лучевая терапия, проводимая на область молочной железы и региональные зоны, не оказывает прямого негативного влияния. Однако при использовании варианта пересадки свободного лоскута, когда в качестве донорских сосудов используются артерии и вены, проходящие в зонах регионального метастазирования и попадающие в поле облучения, факт возможного постлучевого изменения тканей может иметь решающее отрицательное значение. В нашем исследовании из 21 случая использования свободного лоскута после проведения лучевой терапии на область молочной железы и региональные зоны, в 9 случаях доза облучения составила 40 Гр и более. У всех 9 пациенток были выполнены отсроченные реконструкции. При этом у 1 из 9 больных имелся случай полного некроза лоскута в результате тромбоза артериального анастомоза, и ещё 1 случай изменения плана операции ввиду выраженных постлучевых изменений сосудов. Полученный опыт позволяет сказать, что влияние лучевой терапии на результат реконструкции зависит от варианта ректо-абдоминального лоскута. При пересадке свободного лоскута в случае наличия в предоперационном анамнезе указания на лучевую терапию в дозе 40 Гр и более в области сосудов, планируемых для наложения анастомозов, существует риск их повреждения. В этом случае рекомендуется выбрать для соединения сосуды, не вошедшие в зону облучения или осуществить перемещение TRAM-лоскута на 2-х мышечных ножках.
Противоопухолевые цитостатические препараты способны повреждать с разной частотой практически все нормальные структуры организма человека. В литературе имеются противоречивые данные по проблеме совместимости пластического этапа хирургического лечения при раке молочной железы с химиотерапией. В нашем исследовании, при сравнении всех больных, которым химиотерапия была проведена перед реконструкцией (50 человек) с группой больных без химиотерапии (66 человек), не было получено достоверного различия в количестве осложнений (p>0,05). Однако у больных которым в течении 12 месяцев перед операцией в ходе лечения применялась химиотерапия в объёме 6 и более курсов имелось статистически достоверное (p<0,05) увеличение общего количества некрозов лоскута. А также увеличение доли глубоких некрозов абдоминальной донорской зоны по сравнению с больными без химиотерапии перед реконструкцией.
Учитывая, что отдельно взятые неблагоприятные предоперационные условия могут наблюдаться у одного пациента, для отдельного анализа была взята группа больных, у которых имелось сочетание нескольких системных факторов риска. В эту группу вошли 22 пациентки, у которых было два и более системных факторов риска: ожирение (индекс массы тела более 29 кг/м2), курение, проведение химиотерапии в объёме 6 курсов и более в сроки менее 12 месяцев перед операцией. Для сравнения были взяты 45 больных, не имевших системных факторов риска.
Группа пациенток с сочетанием системных факторов риска имела значительно большее количество осложнений и по лоскутам, и по абдоминальной зоне в сравнении с группой без факторов риска. Это позволило сделать вывод, что наличие сочетания системных факторов риска является противопоказанием к применению ректо-абдоминального лоскута с целью восстановления формы груди. Отсутствие факторов риска позволяет полностью исключить наличие глубоких некрозов и снизить количество поверхностных краевых некрозов до 6,6% со стороны лоскута и до 4,4% со стороны донорской абдоминальной зоны.
Таким образом, выбор пациентов для реконструкции молочной железы TRAM-лоскутом с отсутствием системных факторов риска, учёт индивидуальных особенностей анатомии сосудистой сети донорской и реципиентной зоны при выборе варианта операции, а также оценка кровоснабжения трансплантата в ходе операции позволяет снизить до минимума риск возникновения поверхностных и полностью исключить возникновение глубоких послеоперационных некрозов.
Литература
- Бурлаков А.С. Микрохирургические или традиционные методы реконструкции в онкологии. Проблема выбора // Материалы VII конгресса по пластической, реконструкции хирургии и онкологии, г. Москва, 28-30 ноября 2004г.
- Васильев Ю.С. Оптимизация планирования и выполнения пластических операций у больных раком молочной железы: Авторефер. дис… канд. мед. наук – Челябинск, 2004. – 23 с.
- Крохина О.В., Соболевский В.А., Егоров Ю.С. Варианты реконструктивных операций при раке молочной железы // Материалы X Российского онкологического конгресса, г. Москва, 2006 г. - С.115-117.
- Кулишов В.А., Кулишов И.В. Реконструктивно-восстановительные и органосохраняющие операции в комплексном лечение рака молочной железы // Материалы VII конгресса по пластической, реконструктивной хирургии и онкологии, г. Москва, 28-30 нояб. 2004 г. – С. 17 - 18.
- Лактионов К.П., Блохин С.Н., Котов В.А. Выбор метода реконструктивных операций при раке молочной железы. - М., 2004. – 143 с.
- Пак Д.Д., Рассказова Е.А. Одномоментная пластика молочной железы у больных раком // Материалы Российской научно-практической конференции: новые технологии в онкологической практике, г.Барнаул, 2005 г. - С. 46-47.
- Жерлов Г.К., Клоков С.С., Миронова Е.Б. Первичная реконструкция с использованием TRAM –лоскута в комплексном и комбинированном лечении рака молочной железы // Материалы V Всеросс. съезда онкологов: высокие технологии в онкологии, г. Ростов на/Д., 2000г. - Т.3. - С. 126-127.
- Кузнецов А.В. Реконструкция молочной железы ректо-абдоминальным лоскутом у онкологических больных: Дисс… канд. мед. наук. - М., 2006.
Таблица 1
Количество послеоперационных некрозов при различных вариантах реконструкции ректо-абдоминальным лоскутом.
|
Вид операции |
Количество операций |
Некроз лоскута |
Некроз абдоминальной области |
||
|---|---|---|---|---|---|
|
краевой |
глубокий |
краевой |
глубокий |
||
|
TRAM на 2-х ножках |
n=48 (100 %) |
11(22,9%) |
5(10,4%) |
5(10,4%) |
6(12,5%) |
|
16(33,3%) |
11(22,9%) |
||||
|
Свободный TRAM |
n=52 (100 %) |
5(9,6 %) |
1(1,9 %) |
7(13,4%) |
3(5,8%) |
|
6(11,5%) |
10(19,2%) |
||||
|
TRAM на 1-ой ножке |
n=10 (100 %) |
1(10%) |
4 (40%) |
2(20%) |
0 |
|
5 (50%) |
2(20 %) |
||||
|
TRAM с подкачкой |
n=1 (100 %) |
0 |
0 |
0 |
0 |
|
Вертикальный лоскут |
n=5 (100 %) |
1(20%) |
0 |
1(20%) |
0 |
|
1(20%) |
1(20%) |
||||
|
Все случаи: |
n=116 (100 %) |
18(15,5%) |
10(8,6 %) |
15(12,9%) |
9(7,8%) |
|
28(24,1%) |
24(20,7%) |
||||
Таблица 2
Соотношение осложнений у больных, с сочетанием системных факторов риска и больных без факторов риска.
|
Группы риска
|
Некроз лоскута |
Некроз донорской зоны |
|||
|---|---|---|---|---|---|
|
краевой |
глубокий |
краевой |
глубокий |
||
|
Сочетание факторов риска n=22 (100%) |
8 (36,4%) |
5(22,7%) |
5(22,7%) |
6 (27,3%) |
|
|
13 (59,1%)* |
11 (50%)** |
||||
|
Без факторов риска n=45 (100%) |
3 (6,6%) |
0 (0%) |
2 (6,6%) |
0 (0%) |
|
|
2 (6,6%)* |
2 (4,4%)** |
||||
* - p<0,01; ** - p<0,01


